| Головна » 8 клас » Хімія |
Цілі уроку: ознайомити учнів з фізичними властивостями основ; закріпити знання про класифікації основ на розчинні й нерозчинні; розширити знання учнів про хімічні властивості класів неорганічних сполук на прикладі основ; показати дію лугів на індикатори; розвивати навички складання рівнянь хімічних реакцій на прикладі хімічних властивостей основ. Тип уроку: поглиблення й розширення знань. Форми роботи: розповідь учителя, демонстраційний експеримент, лабораторні досліди, робота з опорною схемою. Обладнання: Періодична система хімічних елементів Д. І. Менделєєва, таблиця розчинності, таблиця «Правила техніки безпеки в кабінеті хімії», ряд активності металів, хімічні реактиви.
ХІД УРОКУ
І. Організація класу
ІІ. Аналіз тематичного оцінювання Робота з класом зі з’ясування типових помилок, індивідуальна робота над помилками.
ІІІ. Актуалізація опорних знань, мотивація навчальної діяльності
1) Взаємодія з кислотами. 2) Взаємодія з кислотними оксидами. Додаємо: 3) Взаємодія із солями. І за цим планом будемо вивчати властивості основ.
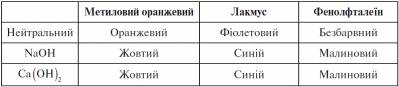
IV. Вивчення нового матеріалу 1. Лабораторна робота № 3. Дія лугів на індикатори Для проведення цієї лабораторної роботи ми використаємо пластинку для мікрометоду. Акуратно в перший ряд капаємо по дві краплі натрій гідроксиду, у другий ряд - по дві краплі кальцій гідроксиду. Далі в перше заглиблення з кислотами додаємо одну краплю метилового оранжевого, у друге - одну краплю лакмусу, у третє - одну краплю фенолфталеїну. На основі спостережень заповнюємо таблицю.
Висновок. У розчинах лугів метиловий оранжевий набуває жовтого забарвлення, лакмус - синього, фенолфталеїн - малинового. Отже, розчини лугів можна визначити з допомогою індикатора. 2. Демонстрація 7. Хімічні властивості основ На початку уроку ми припустили, які властивості повинні мати основи. Подивимося практично.
Дослід 1. Взаємодія лугів з кислотними оксидами Збираємо прилад для одержання вуглекислого газу. Одержаний газ пропускаємо крізь розчин кальцій гідроксиду. - Яку ознаку реакції спостерігаємо? (Випадіння осаду) Записуємо рівняння реакції: CO2+Ca(OH)2→CaCO3+H2O Укажіть тип реакції. (Реакція обміну)
Дослід 2. Взаємодія лугів з кислотами
У дві пробірки наливаємо NaOH і Ca(OH)2, додаємо фенолфталеїн. А потім по краплях знебарвлюємо розчин хлоридною кислотою. Пропонуємо учням записати рівняння реакцій: NaOH+HCl→NaCl +H2O Ca(OH)2+2HCl→CaCl2+2H2O
Дослід 3. Взаємодія лугів із солями У дві пробірки наливаємо CuSO4, Al2(SO4)3 , потім по краплях додаємо розчин їдкого натру. - Які ознаки реакції спостерігаємо? (Утворення нерозчинного осаду) Запишемо рівняння реакції: CuSO4+2NaOH→NaSO4+Cu(OH)2↓ Al2(SO4)3+6NaOH→ 2Al(OH)3+3Na2SO4↓ Усі наші припущення про властивості лугів підтвердилися практично. (Розглядаємо відповідно до пунктів плану.) На основі цього вносимо доповнення в таблицю «Взаємозв’язок між класами неорганічних сполук».
V. Закріплення вивченого матеріалу Керована практика Завдання 1. Здійснити перетворення: CaO→Ca(OH)2→CaSO4←H2SO4←SO3 Знання властивостей класів неорганічних сполук дозволяє нам припустити, з допомогою яких реакцій можна одержати ту чи іншу речовину. Два учні з двох боків: CaO+H2O→Ca(OH)2 Ca(OH)2+H2SO4→CaSO4+2H2O SO3+H2O→H2SO4 H2SO4+Ca(OH)2→CaSO4+H2O Завдання 2. Здійснити перетворення: а) Mg→MgO→Mg(NO3)2→Mg(OH)2 б) Ba→BaO→Ba(OH)2→Ba(NO3)2
VI. Домашнє завдання Опрацювати відповідний параграф підручника, відповісти на запитання до нього, виконати вправи. Здійснити перетворення: BaO→Ba(OH)2→BaCO3←H2CO3←CO2 | |
| Переглядів: 917 | |
Схожі уроки:
| Всього коментарів: 0 | |